Mae gwydnwch AEMWE sy'n cael ei fwydo â dŵr pur yn gymharol isel. Adroddwyd bod foltedd celloedd AEMWEs wedi'u cataleiddio â asgwrn cefn ferrite wedi cynyddu o 1.6 V i 1.75 V mewn 3 awr ar 200 mA/cm2 a thymheredd yr ystafell, er mewn arbrofion electrod disg cylchdroi (RDE), arhosodd gweithgaredd OER y catalydd yn sefydlog drosodd. 4100 o oriau. Adroddwyd hefyd bod iridium ocsid AEMWE wedi'i gataleiddio ar 200 mA/cm2 a 50 gradd wedi cynyddu'r foltedd o 1.75 V i 2.3 V mewn 35 awr, er na wnaethant arsylwi swyddogaetholi piperidine (piperidinium-functionized) AEM heb unrhyw ddiraddio sylweddol.Since mae gweithredu AEMWE gyda dim ond dŵr pur sy'n llifo heb electrolyt hylif ychwanegol yn llai cyrydol, nid oes gan y ffactor cyfyngu mewn gwydnwch AEMWE a gyflenwir â dŵr pur ddim i'w wneud â sefydlogrwydd alcalïaidd y cynulliad MEA, ond yn hytrach â'r gell electrolytig. Mae foltedd gweithredu uchel yn gysylltiedig â dwysedd cyfredol. Yn yr erthygl hon, byddwn yn trafod dau ffactor sy'n cyfyngu ar wydnwch, sef gollwng pilen ïon a gwenwyno o dan amodau foltedd uchel celloedd a dwysedd cerrynt uchel. Mae'r diraddiadau hyn sy'n gysylltiedig â philen ïon yn cael eu cyflymu o dan amodau foltedd celloedd uchel a dwysedd cerrynt uchel.
1. Mae'r bilen ïon yn disgyn oddi ar wyneb y catalydd.
Mae astudiaethau wedi canfod, dros amser, bod y bilen ïon yn gwahanu oddi wrth wyneb y catalydd, gan arwain at ddiraddio perfformiad. Yn eu harbrofion, defnyddiwyd ionomerau polystyren cwaternaidd ag IEC uchel i wella perfformiad AEMWE, gan ddefnyddio cell electrolytig gydag ionomer TMA (IEC=3.3 mequiv/g) ar 2.0 V a 85 gradd. Mae'r dwysedd presennol yn cyrraedd 2.4 A/cm2 (Ffig. 1a). Fodd bynnag, gwelsant ronynnau catalydd yn cael eu fflysio allan o'r ffrydiau allfa anod a catod, gan ddangos nad oedd y bilen ïon uchel-IEC yn gallu angori'r gronynnau catalydd yn yr electrod yn sefydlog yn ystod gweithrediad parhaus. Felly, oes AEMWE gan ddefnyddio TMA{{ Dim ond 7 awr yw 11}} pilen ïon (Ffig. 1b). Ar dymheredd gweithredu is (60 gradd), mae cryfder bondio'r bilen ïon yn cael ei wella, ac mae'r gwydnwch yn cyrraedd tua 12 awr. Er mwyn lleihau colledion perfformiad, cynyddir cryfder bondio'r ionomer ymhellach pan gaiff ei ddefnyddio gyda'r un math o ionomer ar IEC is (TMA-53, IEC=2.6 mequiv./g). Ar dymheredd gweithredu o 60 gradd, roedd foltedd cychwynnol y gell electrolytig ~ 200 mV yn uwch, ond cynyddwyd oes y gell yn sylweddol i 4100 h a gostyngwyd y gyfradd ddiraddio yn fawr, gan nodi cyfaddawd rhwng perfformiad a gwydnwch.
Mae shedding y rhwymwr ionomer yn broblem i ionomerau sydd â gwerthoedd IEC uchel ac amsugno dŵr uchel. O dan amodau hydradol llawn, mae newidiadau maint yr ionomerau hyn yn fwy, a thrwy hynny wanhau adlyniad yr ionomerau i wyneb y catalydd. Mae shedding Ionomer oherwydd rhyddhau nwy yn fwy difrifol yn AEMWE pur sy'n cael ei fwydo â dŵr oherwydd bod ardal rhyngwyneb catalydd-electrolyte AEMWE pur sy'n cael ei fwydo â dŵr yn gymharol fach. Felly, mae'r gollyngiad nwy yn fwy anghydffurf ar ddwysedd cerrynt penodol (Ffig. 1c). Gan fod athreiddedd nwy y deunydd polymer yn llawer is na'r hydoddiant KOH, mae'n anodd tynnu'r nwy anweddol yn gyflym o'r rhyngwyneb ionized catalydd o dan amodau gweithredu cyfredol uchel. Mae gollwng pilenni ïon a achosir gan swigen yn fwy tebygol o ddigwydd yn AEMWE nag yn PEMWE oherwydd bod gan bilenni ïon quaternized hydrocarbyl athreiddedd nwy is ac adlyniad llawer is oherwydd eu bod yn ehangu gormodol mewn dŵr. Arhosodd foltedd celloedd electrolytig AEMWE yn gweithredu ar 100 mA/cm2 yn sefydlog dros 100 awr, ond wrth weithredu ar 300 mA/cm2, methodd y gell o fewn 40 awr, sy'n dangos bod amodau cynhyrchu nwy uwch yn niweidiol i gyflenwad dŵr pur. Mae deunydd AEMWE yn anffafriol. Cafwyd canlyniadau tebyg mewn AEMWE pur a borthir gan ddŵr wedi'i gataleiddio gan haearn hydrocsid nicel.
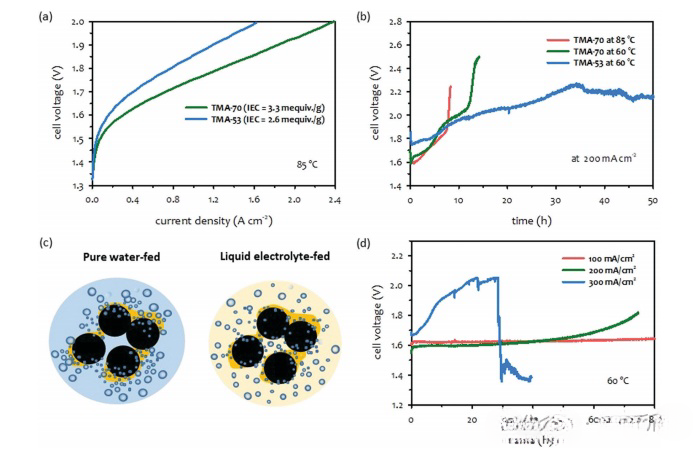
Ffigur 1: Cyfaddawdu perfformiad-gwydnwch AEMWE wedi'i drwytho â dŵr pur. Sylwadau: (AEM: SES-TMA (35um o drwch); pilen ïon: FLN-55; anod: IrO2 (2.5 mg/cm2); catod: PtRu/C (50 wt% Pt, 25wt% Ru, 2mg/ cm Pt). Data AEMWE a gynhyrchwyd yn Labordy Cenedlaethol Los Alamos)
(a) Effaith IEC ionomerau ar berfformiad;
(b) Effaith IEC ionomerau ar berfformiad hirdymor. AEM: HTMA-DAPP (26um o drwch); Anod: Anod: IrO2 (2.5mg/cm2); Cathod: nanofoam NiFe (3mg/cm2).
(c) Diagram sgematig o ryddhau nwy o AEMWE sy'n cael ei fwydo gan ddŵr pur ac wedi'i fwydo gan hylif hylif ar ddwysedd cerrynt uchel.
(d) Effaith dwysedd cerrynt ar berfformiad hirdymor.
Strategaethau i liniaru diraddio a achosir gan shedding bilen yw defnyddio pilenni â gwerthoedd IEC isel a gweithredu ar dymheredd gweithredu isel, er y disgwylir perfformiad llai sylweddol. Fel arall, gellir datblygu ionomerau IEC uchel gydag amsugno dŵr isel i gymedrol. Mae strategaethau synthesis polymer i gyflawni ionomerau hydroffobig chwydd dŵr isel yn cynnwys cyflwyno polycations, rhyngweithiadau pegynol, a chroesgysylltu.
Yn gyntaf, mae dargludedd amsugno dŵr isel polymerau ïonig cwaternaidd yn lleihau cyfradd (cyfradd) cynhyrchu hydrogen. Yn ail, mae cyflwyno rhyngweithiadau polycationig a grŵp pegynol i bolymerau cwaternaidd yn aml yn lleihau sefydlogrwydd cemegol polymerau ïonig. Yn drydydd, gall y broses synthesis o ionomerau uchel-IEC ag amsugno dŵr isel fod yn fwy cymhleth a drud. Dull arall posibl yw defnyddio gwasgarwyr i wella cadernid y bilen ïonig. Yn gyffredinol, mae gwasgarwyr nad ydynt yn ddyfrllyd yn cynyddu ymlyniad cadwyn polymerau â grwpiau ïonig, gan wella adlyniad a chadernid mecanyddol pilenni ïonig. Mae defnyddio gwasgarwyr gwell hefyd yn caniatáu i'r bilen ïon gael ei ddosbarthu'n fwy cyfartal yn yr electrod, gan ganiatáu ar gyfer rhyddhau nwy mwy gwastad a gwella sefydlogrwydd batri o dan amodau cyfredol uchel. Mae lleihau maint y nanoronynnau catalydd hefyd yn helpu i wneud dosbarthiad adweithiau esblygiad nwy yn fwy unffurf.
2. Gwenwyn Ionomer
Electrochemical oxidation of adsorbed phenyl groups in the ion membrane at oxygen evolution (OER) potential is one of the most prominent durability limiting factors of pure water-fed AEMWE. The study observed that a phenolic compound (the conjugate base of phenol) in a solution of benzyltrimethylammonium hydroxide (BTMAOH) was exposed to an iridium oxide catalyst after being in contact with a reversible hydrogen electrode [RHE] at a voltage of 2.1V for 100 hours. surface. It has also been observed that the formation of phenol also occurs at oxygen reduction potential (>{{0}}.6 V), sy'n effeithio'n andwyol ar oes AEMFC (celloedd tanwydd anionig). Yn gyffredinol, mae ocsidiad electrocemegol grwpiau ffenyl yn fwy niweidiol i electrolyzers na chelloedd tanwydd oherwydd bod foltedd gweithredu'r anod AEMWE (1.4-2.2 V) yn llawer uwch na'r catod AEMFC ({{7}). }.6-1.0 V). Mae Ffigur 2a yn esbonio proses ocsidiad electrocemegol grwpiau ffenyl. Mae'r broses ocsideiddio electrocemegol yn dechrau gydag arsugniad grwpiau ffenyl yn yr ionomer. Gan fod carbon yn cyrydu ar botensial OER uchel, nid oes gan AEMWEs nodweddiadol unrhyw gydran carbon yn yr anod. Fodd bynnag, mae'n heriol i ionomerau fod yn gwbl rydd o grwpiau ffenyl. Mae'r grwpiau ffenyl yn yr ionomerau yn cael eu hamsugno'n hawdd ar wyneb y catalydd oherwydd rhyngweithio da electronau π aromatig y grwpiau ffenyl â'r cwmwl electronau o amgylch yr atomau metel. Mae egni arsugniad y darnau ffenyl yn asgwrn cefn yr ionomer ar yr wyneb platinwm hyd yn oed yn uwch na bensen. Unwaith y bydd y grwpiau ffenyl yn cael eu hadsugno ar wyneb y catalydd (cam 1), mae'r grwpiau ffenyl wedi'u hadsugno'n cael eu ocsideiddio a'u trosi i ffenol (cam 2). Er bod cyrydiad carbon nodweddiadol yn cynhyrchu carbon deuocsid (y cynnyrch cyrydiad carbon terfynol) ar botensial OER nodweddiadol, nid yw'r 1,4-grwpiau ffenyl a amnewidiwyd yn yr ionomerau yn cael eu hocsidio'n hawdd i asid maleig i gynhyrchu carbon deuocsid, ond maent yn parhau i fod yn gyfansoddion ffenolig. Mae'r protonau ffenolig a gynhyrchir yn cael eu dadprotoneiddio'n effeithiol gan ïonau hydrocsid yr amoniwm cwaternaidd i niwtraleiddio'r cyfrwng alcalïaidd (cam 3). Gwerthoedd pKa 2-phenylphenol a 2,2'-biphenol yw 9.6 a 7.6, yn y drefn honno.
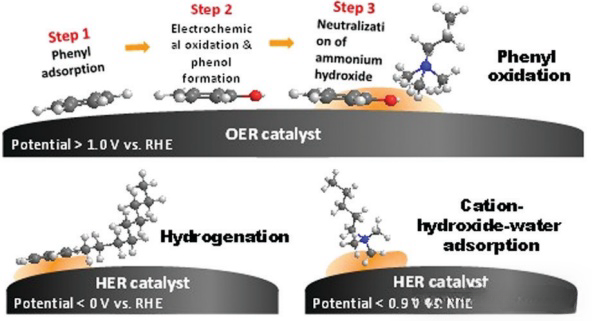
Ffigur 2a: Diagram sgematig o ocsidiad bensen electrocemegol, hydrogeniad a mecanwaith diraddio cyd-arsugno cation-hydrocsid-dŵr.
Gan fod ocsidiad electrocemegol yn digwydd trwy grwpiau ffenyl sydd wedi'u harsugno ar wyneb catalyddion OER, mae egni arsugniad grwpiau ffenyl ar wyneb catalyddion OER yn chwarae rhan hanfodol yn y broses ddiraddio. Canfu damcaniaeth swyddogaethol dwysedd (DFT) fod egni arsugniad grwpiau ffenyl mewn BTMAOH yn gyfochrog â'r arwyneb iridium ocsid yn uwch (1.2 ~ 2.2 eV ar 1.6 V) nag egni La0.85Sr0. 15CoO3 catalydd perovskite. Mae data RDE yn gyson â'r data a gyfrifwyd, hynny yw, mae cyfradd ocsideiddio grwpiau ffenyl ar yr wyneb iridium ocsid tua thair gwaith yn fwy na'r gyfradd ar wyneb catalydd perovskite. Mae Ffigur 2b yn dangos gwydnwch iridium ocsid a perovskite-catalyzed AEMWE gan ddefnyddio bilen ïon HTMA-DAPP. Cynyddodd foltedd celloedd yr AEMWE a gataleiddiwyd iridium ocsid yn gyflym o 1.7 V i 2.1 V o fewn y 5 awr gyntaf o weithredu. Mewn cyferbyniad, arhosodd foltedd yr AEMWE perofskite-catalyzed yn sefydlog ar ~1.8 V am 100 awr.
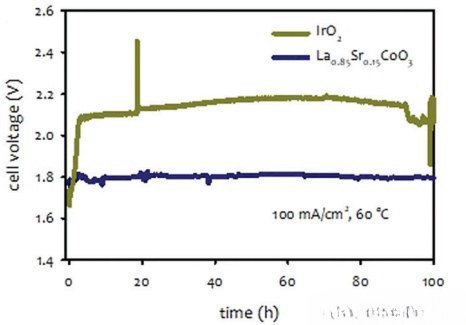
Ffigur 2b: Gwydnwch tymor byr dŵr pur La0.85Sr0.15CoO3 neu IrO2 wedi'i gataleiddio AEMWEs.
Nodiadau: AEM, HTMA-DAPP (35 μm o drwch); ionomer: HTMA-DAPP; anod: La0.85Sr0.15CoO3 (2 mg/cm2) neu IrO2 (1 mg/cm2); catod: Pt/C (0.6 mgPt/cm2). Mesurwyd gwydnwch ar bwysau amgylchynol.
Strategaeth liniaru ar gyfer diraddio grwpiau ffenyl a achosir gan ocsidiad electrocemegol yw defnyddio catalyddion OER gydag egni arsugniad ffenyl is. Er bod egni arsugniad grwpiau ffenyl ar arwynebau metel trawsnewidiol fel platinwm, palladium, neu iridium yn gymharol uchel, gall catalyddion aloi leihau'r egni arsugniad yn sylweddol trwy newid strwythur electronig y ganolfan band-d. Er enghraifft, mae egni arsugniad ffenyl grwpiau BTMA yn gyfochrog ag arwyneb Pt yn -2.30 eV, tra bod egni arsugniad ffenyl grwpiau BTMA yn gyfochrog ag arwyneb Pt1Ru1 yn -1.30 eV. Fel y dangosir yn Ffigur 2b, mae gan y catalydd perovskite nodweddion arwyneb arsugniad ffenyl lleiaf posibl, sy'n fuddiol i weithrediad hirdymor heb achosi gormod o golled perfformiad. At hynny, mae catalyddion perocsid yn llai dibynnol ar pH, a allai fod o fudd i berfformiad AEMWE sy'n cael ei fwydo â dŵr pur. Dull arall yw defnyddio electrolytau polymer ag egni arsugniad is ar gyfer grwpiau ffenyl. Mae egni arsugniad polyolefinau cwaternaidd yn is nag egni polyaromatig cwaternaidd. Mae gan grwpiau ffenyl angylchdroadwy (fel fflworene neu carbazole) egni arsugniad is na grwpiau ffenyl y gellir eu cylchdroi (fel deuffenylau).
Mae Ffigur 2c yn cymharu ymddygiad foltedd tymor byr tri MEAs a wneir o AEMs ac ionomerau â nodweddion arsugniad ffenyl gwahanol, sy'n dangos effaith ocsidiad electrocemegol grwpiau ffenyl ar wydnwch AEMWE. Mae'r MEA cyntaf yn defnyddio HTMA-DAPP ar gyfer yr AEM a'r ionomer. Mae HTMA-DAPP yn cynnwys unedau deuffenyl a terphenyl yn y brif gadwyn, felly mae ocsidiad electrocemegol grwpiau ffenyl yn uchel. Mae'r ail MEA yn cael ei wneud gyda chopolymer tribloc poly (styrene-ethylen-styrene) swyddogaethol trimethylalkylammonium (SES-TMA) AEM ac ionomer HTMA-DAPP. Nid oes gan AEMs SES-TMA grwpiau ffenyl yn asgwrn cefn y polymer, felly mae gradd ocsidiad bensen yn isel. Mae'r trydydd MEA yn cael ei wneud gyda SESTMA AEM ac ionomer poly(fflworene) cwaternaidd (FLN55).
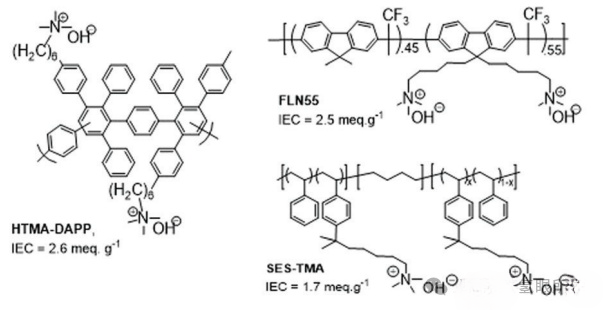
Ffigur 2c: Strwythur cemegol yr electrolyt polymer a ddefnyddir ar gyfer yr astudiaeth ocsidiad bensen.
Gall hydrogeniad darnau pilen a chyd-arsugniad cation-hydrocsid-dŵr cronedig arwain at ddadactifadu electrocatalysyddion CAH, gan effeithio ar berfformiad a gwydnwch dyfeisiau (Ffigur 2a). Er nad yw hydrogeniad rhwymwyr ïon catod AEMWE wedi'i astudio'n systematig ar y lefel un gell, mae hydrogeniad cyfansoddion bensen, ceton, ac olefin ar gatalyddion metel nobl wedi'u dogfennu'n dda. Gall arsugniad hydrocsid cronnol leihau mynediad dŵr i'r wyneb catalydd oherwydd hydoddedd dŵr isel yr haen bilen hydrocsid dwys iawn. Fodd bynnag, mae arsugniad hydrocsid cronnol yn digwydd yn bennaf yn y potensial HOR, sef tua 0.1 V o'i gymharu â RHE, felly gall ei effaith fod yn llai na gwenwyno bilen eraill.
Mae'r ddau ffactor sy'n cyfyngu ar wydnwch AEMWE pur a borthir gan ddŵr yn gysylltiedig â'r rhwymwr ïonig. Gan y bydd y bilen ïonig yn disgyn o'r wyneb electrocatalyst pan nad oes ganddi adlyniad, a bydd gwenwyno pilen ïonig yn digwydd wrth i'r darnau bilen ïonig amsugno ar wyneb catalydd OER, bydd diraddio AEMWE pur sy'n cael ei fwydo â dŵr yn mynd rhagddo ar hyd y naill lwybr diraddio neu'r llall. Oherwydd y cyfaddawd rhwng perfformiad a gwydnwch, mae’n bosibl y bydd cyfraddau cynhyrchu hydrogen is hefyd yn fwy gwydn, sy’n dangos y gallai cyflawni perfformiad uchel a gwydnwch AEMWE pur a borthir gan ddŵr fod yn her dechnegol enfawr wrth ddatblygu system fasnachol hyfyw.
